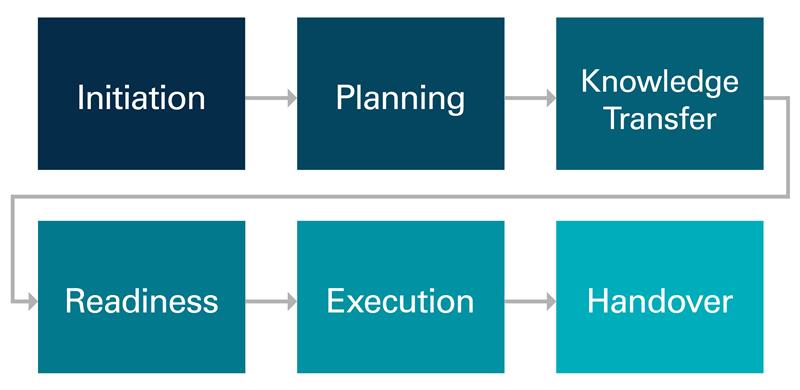
医薬品の技術移転 (TT) プロジェクトでは、準備 段階が極めて重要な役割を果たします。 移行を成功させるための基礎固めである。このフェーズでは、様々な機能にわたる重要な活動の綿密な計画、調整、実行が行われ、それぞれがプロセス性能適格性評価(PPQ)に向けた受入ユニット(RU)の準備に貢献する。
概要
技術移転チームはこのフェーズで、文書化、設備、分析方法を含む必要不可欠なコンポーネントを提供する。前のプロジェクトフェーズで共有された知識により、RUは管理戦略の最終決定、分析方法の適格性確認、必要な設備改造を行うことができる。この段階での活動は、継続的な知識移転(KT)と並行して行われることが多く、文書作成と承認の反復プロセスが必要となる。リスクアセスメントは生きた文書として扱われ、TT プロジェクト期間中、リスク識別及び緩和 戦略の継続的な見直しを促す。プラント能力アセスメントは、PPQ の前に実施され、全体的なプロジェクト計画の一部とし て、予備的な水やエンジニアリングを含む可能性がある。運営委員会は、ステージゲート会議を実施し、すべての要求事項がバッチ実行に適 しているかどうかを決定し、エンジニアリングバッチを進める承認を与える。
主な役割と活動
ビジネス機能
RU ビジネスグループは、すべての人材育成の要件を満たすことに専念します。予算の遵守、発売日、予想数量など、ビジネス目標に向けた TT チームの進捗状況を積極的に監督します。製品移管のために顧客と関わるビジネスグループは、ビジネス戦略の変更を伝え、TT PM がプロジェクトの前提条件とリスクへの影響を評価できるようにします。
技術移転プロジェクト・マネージャー
TT PM は、レディネス段階で指揮を執り、プラントのレディネス要件を実行するすべてのワークストリームとチームメンバーを監視する。コミュニケーション・プランの効果的な実行と調整は、進捗状況の監視、課題への対処、障害の克服のために極めて重要である。TT PM は、TT チャーターに対する変更の影響を継続的に評価し、意思決定を促進し、積極的にリスクを管理する。さらに、TT PM は、全てのバリデーション計画と PPQ 要件の完了を、包括的な TT プロトコルに文書化する。
プロセス機能
プロセスグループは、製品管理戦略を確定するために必要なすべてのデータを得ることに集中する。効果的な管理戦略を展開するためには、プロセス、エンジニアリング、分析、製造の各グループと密接に協力することが不可欠である。プロセスパラメーターとその範囲は通常、ラボバッチと臨床開発段階で得られた知識に基づいて分類される。商業製品の場合、RUはセンダリングユニット(SU)で使用されている既存のコントロール戦略を活用することができる。実験室規模またはパイロット製造規模でのプロセス特性研究は、製品の品質とプロセス効率に関するデザインスペースと故障エッジに関する洞察を提供する。管理戦略を実証する最終エンジニアリングバッチは、PPQ の前に実施されるべきである。プロセスグループはまた、この段階で、サンプリング計画や分析試験戦略を含むプロセス検証プロトコルを作成する。
分析機能
RU 分析グループは、計画段階で作成されたバリデーション計画を実行する。様々な側面をカバーするすべてのメソッドバリデーションおよび/または移管プロトコルが作成され、承認され、実行される。コンペンディアルメソッドはRUで実施され、適合性を検証する。分析グループはまた、ラボまたはパイロットスケールバッチから必要なサンプルを分析することで、プロセスグループをサポートします。
エンジニアリング機能
エンジニアリング・グループは、準備段階におけるすべての設備、ユーティリティ、プロセス、分析機器の設置と適格性確認に責任を負う。工場受入試験(FAT)と施設受入試験(SAT)のためのベンダーとの協力は、仕様への適合を確実にするために極めて重要である。実行段階に進む前に、すべての新しい機器と施設の改造の適格性確認が完了していなければならない。エンジニアリングは、適格性評価プロトコルを作成し、実行し、特定のユニット操作に関するトレーニングを提供し、予防保全計画と予備部品要件をこの段階の終わりまでに組み込む。
製造機能
製造グループは、RUがプロセスを実行するために必要なSOP、作業指示書、バッチ記録を作成する。これらの文書は、要員の訓練に使用され、EHSリスクアセスメントの一部を形成する。製造部門は、工場の施設と設備が使用可能な状態にあることを確認し、レディネス活動中に TT チームを支援し、レディネスを確認するための試験を実施する。次の段階に進む前に、文書化及び訓練要件が最終化され、PPQ への準備が完全に整うようにする。
規制機能
薬事グループは、薬事申請に必要な文書を作成し、入手する。活動には、新情報の評価、保健当局からのフィードバック、製品ラベルの最終化などが含まれる。薬事戦略は、工程管理、バリデーション戦略、市場戦略など、レディネス活動で得られた知見と照らし合わせて評価される。薬事グループはまた、品質グループと協力して承認前検査(PAI)準備計画を策定する。
品質機能
品質グループは、部門間で協力し、コンプライアンスレビューを実施し、PPQ準備のための文書を承認する。品質グループは、PPQの前に、逸脱、CAPA、変更管理を確実に終結させる。品質グループは、PPQバッチリリースの手順を開発し、PAI準備計画について規制部門と協力し、新規ベンダーの認定と材料サプライヤーの監査を行います。
ソーシング/サプライチェーン機能
ソーシング/サプライチェーングループは、TT に必要な資材を発注し、RU システムでのセットアップを確実に行い、品質がタイムリーにリリースできるようにします。設備や資材のニーズを、プロジェクト全体の計画や確立されたリードタイムに合わせることが重要です。
技術移転成功への道
準備段階は、後続の段階、特にPPQのための強固な基盤を確立するために、多様な機能が協力するダイナミックな段階である。ビジネスから規制、品質に至るまで、各グループはRUのシームレスな移行の準備に重要な役割を果たす。この段階を成功させることは、単なる前提条件ではなく、医薬品の技術移転を成功させるために必要な計画と共同作業の集大成である。
CAIの技術移転ブログ・シリーズでは、効果的な技術移転の各ステージについて、以下のように順を追って説明しています。