Nel corso di unprogetto di trasferimento tecnologico (TT) farmaceutico, la fase di preparazione svolge un ruolo fondamentale in quanto stabilisce le basi per una transizione di successo. Questa fase comporta una pianificazione meticolosa, il coordinamento e l’esecuzione di attività chiave in varie funzioni, ognuna delle quali contribuisce alla preparazione dell’Unità Ricevente (RU) per la Qualificazione delle Prestazioni di Processo (PPQ).
Panoramica
In questa fase il team di trasferimento tecnologico fornisce i componenti essenziali, tra cui la documentazione, le attrezzature e i metodi analitici. Le conoscenze condivise nella fase precedente del progetto consentono all’IF di finalizzare la strategia di controllo, di qualificare i metodi analitici e di apportare le modifiche necessarie all’impianto. Le attività di questa fase sono spesso parallele al trasferimento continuo delle conoscenze (KT), rendendo necessario un processo iterativo nello sviluppo e nell’approvazione dei documenti. La valutazione dei rischi viene trattata come un documento vivo, che richiede una revisione continua dell’identificazione dei rischi e delle strategie di mitigazione per tutta la durata del progetto TT. Prima del PPQ viene condotta una valutazione della capacità dell’impianto, che potrebbe comportare una serie di prove preliminari di acqua o di ingegneria come parte del piano generale del progetto. Il comitato direttivo conduce una riunione di stage gate per determinare se tutti i requisiti sono soddisfatti per l’esecuzione del lotto, fornendo l’approvazione per procedere con il lotto di ingegneria.
Ruoli e attività chiave
Funzione aziendale
Il gruppo RU Business si occupa di soddisfare tutti i requisiti di formazione del personale. Supervisiona attivamente i progressi del team TT verso gli obiettivi commerciali, tra cui il rispetto del budget, la data di lancio e il volume previsto. Impegnato con i clienti per il trasferimento del prodotto, il gruppo Business comunica i cambiamenti nella strategia aziendale, consentendo al PM TT di valutarne l’impatto sui presupposti e sui rischi del progetto.
Responsabile del progetto di trasferimento tecnologico
Il PM TT si occupa della fase di preparazione, monitorando tutti i flussi di lavoro e i membri del team che eseguono i requisiti di preparazione dell’impianto. L’esecuzione efficace e il coordinamento del piano di comunicazione sono fondamentali per monitorare i progressi, affrontare le sfide e superare gli ostacoli. Il PM TT valuta continuamente l’impatto delle modifiche sul programma di lavoro TT, facilita il processo decisionale e gestisce attivamente i rischi. Inoltre, il PM TT documenta il completamento di tutti i piani di convalida e i requisiti PPQ in un protocollo TT completo.
Funzione di processo
Il gruppo Processo si concentra sull’ottenimento di tutti i dati necessari per finalizzare la strategia di controllo del prodotto. La stretta collaborazione con i gruppi di Processo, Ingegneria, Analisi e Produzione è essenziale per garantire l’implementazione di una strategia di controllo efficace. I parametri e gli intervalli di processo sono tipicamente classificati in base ai lotti di laboratorio e alle conoscenze acquisite durante le fasi di sviluppo clinico. Per i prodotti commerciali, l’IF può sfruttare una strategia di controllo esistente in uso presso l’unità di spedizione (SU). Gli studi di caratterizzazione del processo su scala di laboratorio o di produzione pilota forniscono indicazioni sullo spazio di progettazione e sui margini di errore per la qualità del prodotto e l’efficienza del processo. I lotti finali di progettazione, che dimostrano la strategia di controllo, dovrebbero essere eseguiti prima del PPQ. In questa fase il gruppo di processo scrive anche i protocolli di convalida del processo, compresi il piano di campionamento e la strategia di test analitici.
Funzione analitica
Il gruppo analitico dell’IF esegue il piano di convalida sviluppato nella fase di pianificazione. Tutti i protocolli di convalida e/o trasferimento dei metodi che riguardano vari aspetti vengono scritti, approvati ed eseguiti. I metodi compendiali vengono eseguiti presso l’IF per verificarne l’idoneità. Il gruppo analitico supporta anche il gruppo di processo analizzando i campioni richiesti da lotti di laboratorio o su scala pilota.
Funzione di ingegneria
Il gruppo di ingegneria è responsabile dell’installazione e della qualificazione di tutti gli impianti, le utenze, i processi e le apparecchiature analitiche durante la fase di preparazione. La collaborazione con i fornitori per i Test di Accettazione in Fabbrica (FAT) e i Test di Accettazione in Sito (SAT) è fondamentale per garantire la conformità alle specifiche. La qualificazione di tutte le nuove apparecchiature e le modifiche agli impianti devono essere completate prima di passare alla fase di Esecuzione. L’ingegneria scrive ed esegue i protocolli di qualificazione, fornisce formazione sulle operazioni specifiche dell’unità e incorpora un piano di manutenzione preventiva e i requisiti per le parti di ricambio entro la fine della fase.
Funzione di produzione
Il gruppo di produzione scrive le SOP, le istruzioni di lavoro e i registri dei lotti necessari all’IF per eseguire il processo. Questi documenti vengono utilizzati per la formazione del personale e fanno parte della valutazione dei rischi EHS. La produzione si assicura che le strutture e le attrezzature dell’impianto siano pronte all’uso, supportando il team TT durante le attività di preparazione e conducendo test per confermare la preparazione. La documentazione e i requisiti di formazione vengono finalizzati prima di passare alla fase successiva per garantire la piena preparazione al PPQ.
Funzione regolatoria
Il gruppo Regulatory redige e ottiene i documenti necessari per la presentazione delle normative. Le attività comprendono la valutazione di nuove informazioni, il feedback delle autorità sanitarie e la finalizzazione delle etichette dei prodotti. La strategia regolatoria viene valutata in base ai risultati ottenuti durante le attività di preparazione, tra cui il controllo dei processi, la strategia di convalida e la strategia di mercato. Il gruppo Regulatory collabora anche con il gruppo Quality per sviluppare un piano di preparazione per le ispezioni pre-approvazione (PAI).
Funzione Qualità
Il gruppo Qualità collabora con tutte le funzioni, eseguendo revisioni di conformità e approvando la documentazione per la preparazione del PPQ. Assicura la chiusura di deviazioni, CAPA e controlli di modifica prima del PPQ. Il gruppo Qualità sviluppa una procedura per il rilascio dei lotti PPQ, collabora con la Regulatory per il piano di preparazione al PAI, qualifica i nuovi fornitori e verifica i fornitori di materiali.
Funzione Sourcing/Catena di fornitura
Il gruppo Sourcing/Supply Chain ordina i materiali necessari per il TT, assicurando la configurazione nei sistemi RU per il rilascio tempestivo da parte della Qualità. È fondamentale allineare le esigenze di attrezzature e materiali al piano generale del progetto e ai tempi di consegna stabiliti.
La strada per un trasferimento tecnologico di successo
La fase di preparazione è una fase dinamica in cui diverse funzioni collaborano per stabilire una solida base per le fasi successive, in particolare il PPQ. Ogni gruppo, da quello commerciale a quello normativo e della qualità, svolge un ruolo fondamentale nel preparare l’IF a una transizione senza soluzione di continuità. Il successo di questa fase non è solo un prerequisito, ma il culmine della pianificazione e degli sforzi di collaborazione necessari per un trasferimento tecnologico farmaceutico di successo.
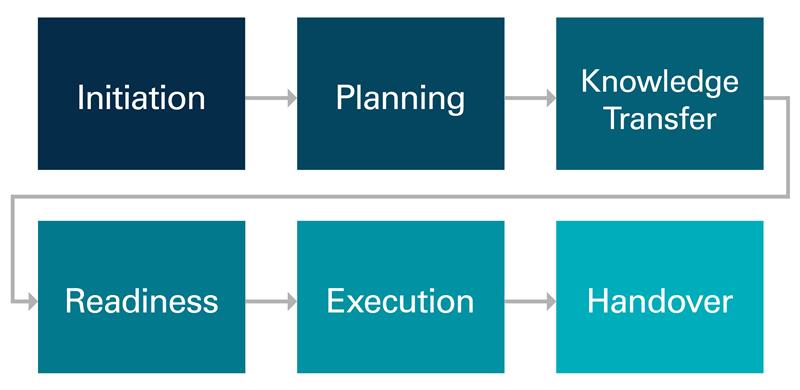
Segui la serie di blog del CAI sul Trasferimento Tecnologico mentre percorriamo tutte le fasi di un trasferimento tecnologico efficace, come illustrato di seguito.